朗沐续签降价幅度好于预期,康弘药业(002773.SZ)股价两日涨近19%
11月28日,国家医保药品目录调整谈判结果正式揭晓,70个药品通过谈判新增进入医保目录,包括52个西药和18个中成药,价格平均降幅为60.7%,还有27个药品“续约”成功,合计97个药品纳入医保目录。
当日晚间,康弘药业(002773.SZ)便发布公告称,公司的康柏西普眼用注射液(商品名为朗沐)纳入了《国家基本医疗保险、工伤保险和生育保险药品目录(2019年版)》。
11月29日,该公司的股价在昨日涨停的基础上再度高开8%并迅速被拉升至涨停。不过,其股价此后几度破板,截至今日收盘最终上涨7.92%,两日涨幅达18.71%,报收39.78元/股,全天成交10.55亿元,最新总市值为348.31亿元。
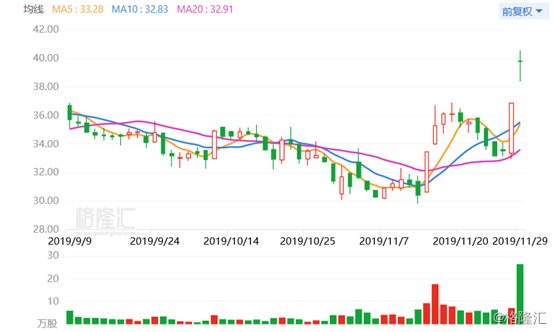
(图片来源:格隆汇)
资料显示,成都康弘药业集团股份有限公司上市于2015年6月,公司的主营业务为药品(包括生物制品、中成药、化学药)和医疗器械(主要是眼科医疗器械)的研发、生产与销售,其中前者是上市公司的业绩支柱。
2019年半年度业绩报告显示,该公司的上市产品主要有康柏西普眼用注射液、松龄血脉康胶囊、舒肝解郁胶囊、渴络欣胶囊、胆舒胶囊、一清胶囊、盐酸文拉法辛缓释片、阿立哌唑口崩片、枸橼酸莫沙必利分散片、右佐匹克隆片等十二个药品和一个医疗器械。
截至2019年9月30日,该上市公司的控股股东为成都康弘科技实业(集团)有限公司,实际控制人则是柯潇、柯尊洪、钟建荣。
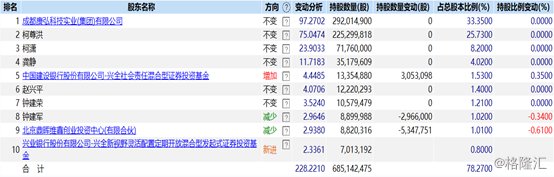
(图片来源:Wind)
公告显示,康弘药业旗下的康柏西普眼用注射液(商品名:朗沐)的适应症包括50岁以上的湿性年龄相关性黄斑变性(AMD);糖尿病性黄斑水肿(DME)引起的视力损害;脉络膜新生血管(CNV)导致的视力损害。
此款产品规格为0.2ml/支,2017年入选的价格是5550元,而此次续签价格降至4160元,降幅为25.05%,好于市场预期;支付标准有效期为2020年1月1日至2021年12月31日。
据悉,康柏西普眼用注射液是一款抗VEGF药物,是当下视网膜疾病的主要治疗药物之一。
资料显示,视网膜疾病是一种视网膜在各种因素下发生病变如出血、渗出物、增生或水肿的眼部疾病,主要包括湿性年龄相关性黄斑病变(wAMD)、糖尿病性视网膜病变(DR)、糖尿病性黄斑水肿(DME)、视网膜静脉阻塞(RVO)和近视的脉络膜新生血管形成(mCNV)。
除了康弘药业的康柏西普眼用注射液外,国内已上市的抗VEGF药物还有进口药物雷珠单抗、阿柏西普两款产品。

(图片来源:Wind)
据悉,阿柏西普此次新进入医保,纳入AMD和DME这两个最大的适应症,而雷珠单抗同样续约成功,比康柏西普更多纳入一个“继发于视网膜静脉阻塞(RVO)的黄斑水肿引起的视力损害”适应症。不过,本次雷珠单抗与阿柏西普均未公布医保支付价格。
康弘药业昨日发布的公告还显示,每眼第1年度最多支付5支(阿柏西普、雷珠单抗以及康柏西普合并计算),原先为1年限4支,该调整超预期。
实际上,该上市公司的康柏西普在2017年通过谈判首次纳入国家医保时的报销适应症仅覆盖AMD适应症,国内患者数约300万人。此次续签,该款产品新增DME、CNV两个适应症,对应国内约600万患者,理论上医保覆盖人数扩至原先3倍。
事实上,在朗沐上市前,该上市公司的收入主要来源于化学药与中成药。而在该产品自2014年上市以来,其优异的市场表现使其成为公司增长的主要产品。
具体而言,该产品上市第一年的销售收入为0.74亿元,随后四年其销售收入快速增长,分别为2.67亿元、4.76亿元,6.18亿元、8.82亿元。
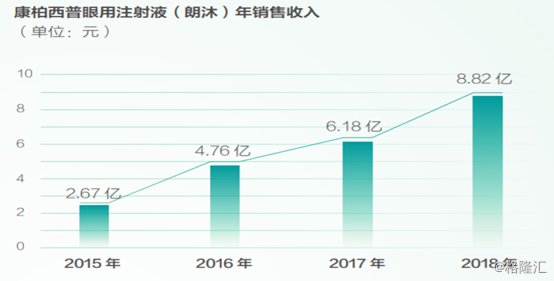
(图片来源:Wind)
作为对比,2015年至2018年,康弘药业实现的营收分别为20.74亿元、25.4亿元、27.86亿元、29.17亿元,朗沐的营收在当期总营收中的占比分别为12.87%、18.74%、22.18%、30.24%。
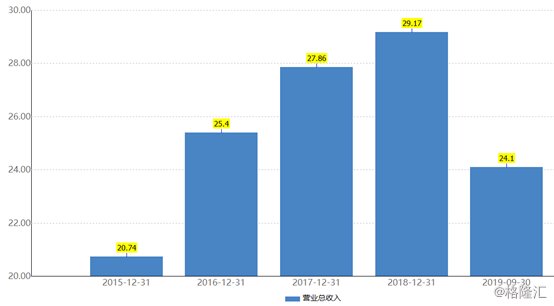
(图片来源:Wind)
不难发现,该款产品实现的营收持续增长,在上市公司的总营收中的占比也是逐年提高的,2018年时甚至超过了3成。
如今,新增DME、CNV两个适应症,康柏西普产品或将迎来放量,进一步提升上市公司的业绩。
值得一提的是,康柏西普的RVO适应症正在国内进行3期临床,康弘药业未来有望完成4大适应症全覆盖。
不过,从目前的情况来看,虽然该上市公司的产品降价幅度要好于市场预期,而且纳入医保目录将有利于该产品的销售,但是其股价在近两日大涨还是短线资金的炒作行为。
值得注意的是,进入2019年以来,康弘药业的一些股东、高管减持了手中的持股。
据不完全统计,包括北京鼎晖维鑫创业投资中心(有限合伙)、天津鼎晖元博股权投资基金(有限合伙)、钟建蓉在内的股东减持了5039.62万股,减持市值达到了18.27亿元。

(图片来源:Wind)
